学科动态
傅开元、王衣祥研究团队发表论文解析颞下颌关节盘移位后发生髁突骨吸收的新机制
近日,北京大学口腔医院医学影像科傅开元教授和中心实验室王衣祥研究员团队在JCI insight发表题为 Increased joint loading induces subchondral bone loss of temporomandibular joint via the RANTES-CCRs-Akt2 axis的研究论文。该研究深入揭示了关节盘移位产生的应力过载在颞下颌关节髁突骨吸收过程中的调控机制,并阐述了应力过载激活的RANTES-CCRs-Akt2轴在破骨分化中的关键作用,为颞下颌关节骨关节炎的早期防治提供了新思路。
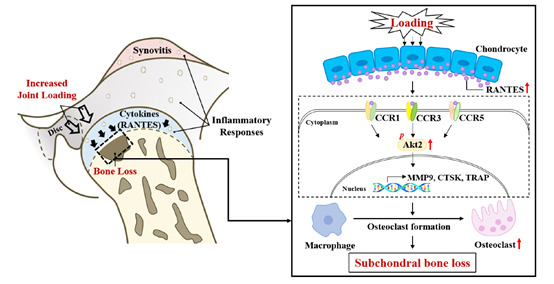
关节盘移位致髁突骨吸收分子机制的示意图
颞下颌关节骨关节炎(temporomandibular joint osteoarthritis, TMJOA)是以关节软骨退行性变及软骨下骨改建为病理特征、疼痛和功能障碍为临床表现的慢性疾病。其中,TMJOA早期通常表现为髁突表面的骨质吸收、破坏。既往的研究发现,不可复性关节盘移位是引起TMJOA髁突骨吸收的重要因素。但是,由于缺乏合适的动物模型和检测手段,目前尚不清楚关节盘移位后髁突骨吸收的发生机制。
鉴于此,课题组通过建立关节盘移位致TMJOA的动物模型和小动物关节面压力监测系统,发现关节盘移位使髁突表面压力显著升高,并伴随相应部位软骨下骨质丢失。
为深入探究应力过载导致髁突骨吸收的分子机制,研究人员通过建立离体髁突组织块的体外加压培养模型,发现关节盘移位引起的应力过载可以激活RANTES-CCRs-Akt2轴并促进破骨细胞形成,从而在髁突软骨下骨吸收中发挥关键作用;抑制RANTE-CCRs-Akt2轴可以减少破骨细胞形成、缓解髁突骨吸收、改善软骨下骨微结构。进一步地,研究人员通过高通量测序及ELISA验证,发现趋化因子RANTES与髁突吸收关系密切,可以作为临床中预测早期TMJOA的生物标志物。
综上,该研究从一个全新的角度认识了TMJOA的发生机制,提出关节盘移位产生的异常应力激活RANTES-CCRs-Akt2通路促进的破骨分化是早期TMJOA发生的生物学机制,有望将来为TMJOA的防治提供新思路。
文献链接:
https://insight.jci.org/articles/view/158874
作者简介:
课题组博士后冯诗阳为本文的第一作者,傅开元教授和王衣祥研究员为共同通讯作者。该研究受到国家自然科学基金(82170979)和北京大学口腔医院国家临床重点专科建设项目(PKUSSNKP-202103)的资助。

傅开元教授现任北京大学口腔医学院医学影像科主任,兼任中华口腔医学会颞下颌关节病学及𬌗学专业委员会主任委员、北京口腔医学会口腔颌面影像学专委会主任委员。以第一作者和通讯作者发表论文120余篇,其中SCI收录60余篇,主编专著2本,参编专著或教材20本。

王衣祥,研究员,博导,北京大学口腔医院中心实验室副主任,细胞平台、生物样本库及基因编辑小鼠平台负责人、中华口腔医学会生物医学专委会委员。
主要研究领域:口腔肿瘤、遗传病和炎症性疾病的发病机制。
以第一和通讯作者身份发表学术论文70余篇,获得2016年教育部高等学校科学研究优秀成果奖—自然科学科学二等奖、2017年北京医学科技奖三等奖、2018 年中华口腔医学会科技奖二等奖、2018年北京市科学技术奖三等奖、和2020年中华口腔医学会科技奖三等奖各1项。












 我想进修
我想进修 环境信息公开
环境信息公开 招聘信息
招聘信息 临床实验者招募
临床实验者招募 急诊就医
急诊就医 我想住院
我想住院 结果查询
结果查询 我想表扬
我想表扬 意见反馈
意见反馈